典型的兰卡杀菌素(lankacidins,1-4)是一类具有十七元大环内酯结构的聚酮肽杂合类抗生素。其独特且高度化学敏感的桥连多取代戊内酯结构单元以及重要的生理活性吸引了国际上多个化学合成研究组的关注。迄今为止,对保留戊内酯的大环家族成员的全合成路线仅有两条,即美国罗切斯特大学Kende小组于1993年首次报道的lankacidin C的全合成(线性最长34步)以及上海有机所洪然课题组于2017年报道的lankacidinol的仿生合成(线性最长8步)。2018年,东北农业大学的王相晶等人从链霉菌Streptomyces sp. HS-NF-1178的发酵液中分离到了两种不具备C2-C18单键连接的抗肿瘤抗生素2,18-seco-lankacidinols A和B(5和6,如图1所示)。加州大学旧金山分校的Seiple小组于同年实现了长链2,18-seco-lankacidinol B的化学合成,并将天然产物立体化学修正为原先提出的C4-差向异构体(7)。本项工作则计划通过对另一个具有独特C18-O半缩醛胺结构的复杂大环家族成员2,18-seco-lankacidinol A(5)开展全合成,解决分离工作中尚未完成的C18立体化学鉴定问题,同时进一步确定戊内酯部分的立体化学是否与之前典型的兰卡杀菌素家族成员相关。
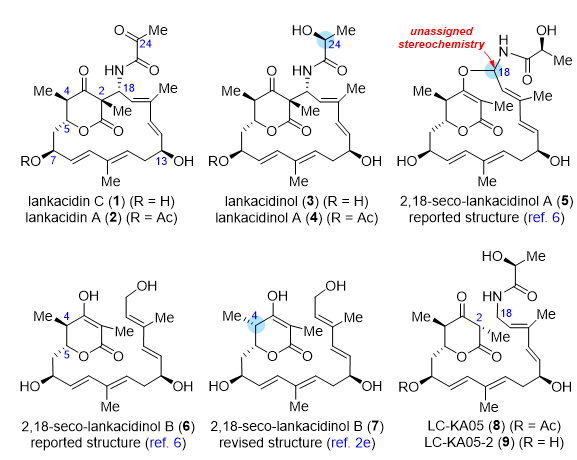
图1. 兰卡杀菌素家族天然产物结构举例
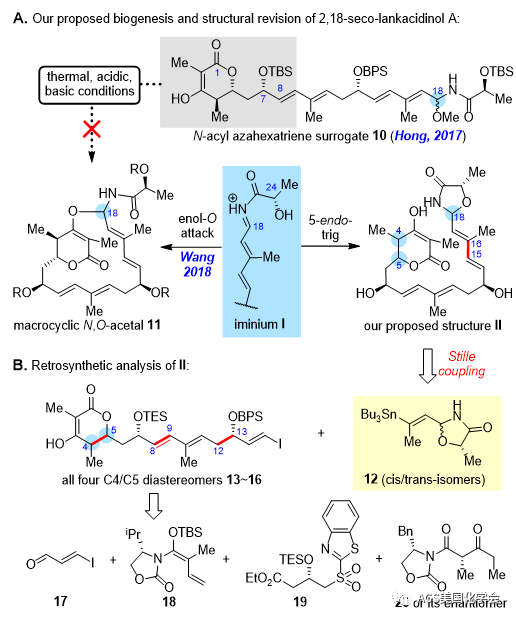
图2. 2,18-seco-lankacidinolA修正结构的提出和逆合成分析
使用本课题组在lankacidinol合成中仿生Mannich大环环化反应底物10(Hong, et al. J. Am. Chem. Soc. 2017, 139, 12939),尝试通过反应条件的改变来调控烯醇进攻的化学选择性以获得相应N,O-缩醛大环产物11,遗憾的是各种尝试均没有成功。在这一过程中对C7位硅基脱除的长链副产物进行核磁共振氢谱信号归属时,意外发现它们与目标天然产物骨架C1-C8部分吻合较好。在重新分析了分离文献中提供的二维核磁共振数据后,作者认为2,18-seco-lankacidinol A中的N,O-缩醛结构在生物合成中可能是由N-乳酰侧链OH进攻亚胺阳离子中间体I形成,进而提出天然产物的真实骨架可能是含有1,3-噁唑啉-4-酮结构的长链II(如图2所示)。为了验证这一设想,作者采用高度汇聚的策略将不同立体化学的戊内酯烯基碘异构体分别与两种C18构型的噁唑啉酮锡试剂片段进行偶联。工作的难点在于后者的合成,在热裂解或者绝大多数酸性条件下N-乳酰基-N,O-缩醛25在形成亚胺后易于发生质子解脱锡、烯酰胺异构化或双键顺式异构化等各种副反应。通过细致地筛选反应条件,作者发现在室温下以四氢呋喃为溶剂、分子筛为添加剂、对甲苯磺酸吡啶盐(PPTS)作为催化剂时,以中等收率获得所需5-endo-trig的两个C18非对映异构的环化产物(trans/cis, 1:3,如图3所示)。戊内酯烯基碘片段13的合成由3-碘丙烯醛17出发依次连接三个模块快速获得,需要注意的是在进行Stille反应片段连接之前,两个硅醚保护基需要提前进行脱除。作者最后发现由脱硅产物32与次要trans-12进行偶联后得到的4R,5R,18S-长链非对映异构体37,其核磁共振波谱数据与天然产物报道数据一致,从而完成了2,18-seco-lankacidinol A的全合成与结构修正,也支持了作者修正的生源合成假说。
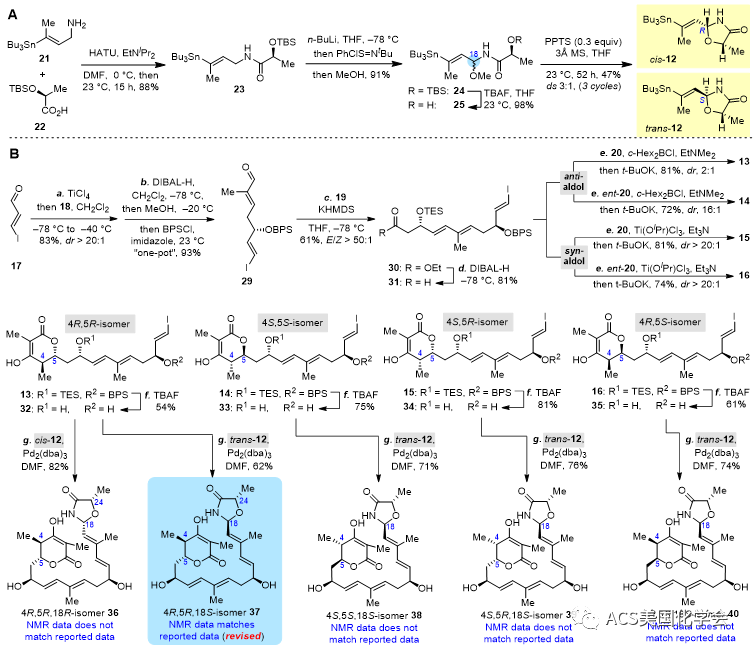
图3. 2,18-seco-lankacidinolA若干非对映体的合成以及结构修正
该研究成果近期发表于Organic Letters,并入选ACS Editors' Choice。本项目得到了国家自然科学基金重大研究计划重点项目(National Natural Science Foundation of China, 91856202) 等项目的支持。


